Fósforo: Compreenda os diferentes tipos de fósforo e como medir níveis de (P) em amostras de água e esgoto
Compreender diferentes formas de fósforo e diferentes métodos de medição pode se tornar confuso. Este artigo ajudará você a entender melhor como medir os níveis de fósforo em amostras de água e esgoto. Por sua vez, também ajudará você a entender as diferentes formas de fósforo, os diferentes métodos de teste e as razões por trás do uso dos diferentes métodos de medição. Isso permitirá uma melhor comunicação e interpretação dos resultados ao realizar testes de fósforo.
Fosfatos versus fósforo
A quantidade de fosfato pode ser expressa de duas maneiras diferentes:
• Fosfato (PO₄³-) também conhecido como ortofosfato, ou
• Fósforo (P) também conhecido como ortofosfato como fósforo (PO₄-P).
Ortofosfato
O ortofosfato é uma molécula com um átomo de fósforo cercado por quatro átomos de oxigênio e possui uma carga negativa de três (Figura 1).
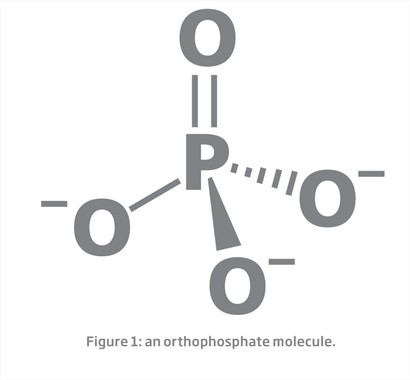
Então, fosfato ou ortofosfato é uma medida da quantidade de moléculas de ortofosfato (PO (³³) em uma amostra. Enquanto fósforo ou ortofosfato como fósforo (PO₄-P), é uma medida da quantidade de íons de fósforo) (P) em uma amostra Isso significa que, quando o fosfato é medido, os quatro átomos de oxigênio ligados ao átomo de fósforo são incluídos na medição, enquanto que ao medir o fósforo, eles não são incluídos.
A maioria dos testes de fosfato ou fósforo é na verdade uma medida de ortofosfato, também conhecido como fósforo reativo.
No entanto, é possível converter facilmente entre as duas medidas com uma simples multiplicação ou divisão. Para converter um resultado de fósforo (P) em fosfato (PO₄³-), basta multiplicar por 3,06. Pelo contrário, para converter de fosfato em fósforo, você só precisa dividir por 3,06. A razão pela qual isso funciona é porque a molécula de ortofosfato (PO3³) é aproximadamente 3,06 vezes mais pesada que o átomo de fósforo (P).
Você pode determinar esse fator calculando primeiro o peso molecular do ortofosfato (PO₄³³-). O peso atômico do oxigênio é de aproximadamente 16 um e existem quatro átomos de oxigênio em uma molécula de ortofosfato. Enquanto o peso atômico do fósforo é de 31 amu e existe um átomo de fósforo em uma molécula de ortofosfato. Então, o peso molecular do ortofosfato (PO (³-) é:
16 * 4 + 31 = 95 amu.
Então, para encontrar a quantidade de fósforo em cada molécula de fosfato, basta dividir o peso molecular do ortofosfato (PO3³) pelo peso atômico do fósforo:
95/31 = 3,06.
Em outras palavras, 1,0 mg / L de fósforo (como P) = 3,06 mg / L de fosfato (PO3-). A leitura de 10 mg / L de fosfato (PO3-) é igual a 3,26 mg / L de fósforo (como P).
Formas de fosfato / fósforo
Como mostrado, fosfato e fósforo são intercambiáveis, com a diferença de que uma medida é o composto, enquanto a outra é elementar. Para fins de medição do fosfato, ele pode ser dividido em três categorias: ortofosfatos, fosfatos condensados e fosfatos orgânicos. No entanto, a única forma de fosfato que é realmente medida colorimetricamente é o ortofosfato. Todas as outras formas devem ser convertidas em ortofosfato para que a reação colorimétrica ocorra.
Para medir os fosfatos condensados ou fosfatos orgânicos, eles devem se tornar ortofosfatos. Isso é feito por digestão com um ácido e / ou oxidante a uma temperatura muito alta usando um digestor em bloco.

Figura 2: Digestor para frascos de 16 mm
Metodologia personalizada Ortofosfato (fosfato / fósforo): os métodos de aminoácido, molibdovadadadato e ácido ascórbico
03 métodos para medir a concentração de ortofosfato em uma amostra:
1.- Método de aminoácidos , que é uma adaptação dos métodos padrão para o exame de água e esgoto.
2.- Método Molibdovanadato , que é uma adaptação dos Métodos Padrão para o Exame de Águas Residuais e Águas Residuais, edição 23, 4500-PC, método do ácido vanadomolibdofosfórico.
3.- Método do ácido ascórbico , que é uma adaptação do método EPA 365.2 e dos Métodos Padrão para o Exame de Águas Residuais e Águas Residuais, edição 20, 4500-PE, método do ácido ascórbico.
Os métodos de aminoácidos e molibdovanadato (também chamados vanadomolibdofosfórico) são para medições de alta concentração. O método de aminoácidos é um método comum usado e os medidores que usam esse método medem até 30 mg / L de fosfato e 15 mg / L de fósforo.
Medidores que usam o método molibdovanadato
Os medidores que usam o método molibdovanadato podem medir o fósforo até 32,6 mg / L ou cerca de 100 mg / L como fosfato. O método do ácido ascórbico é útil para medições de fosfato / fósforo de baixo alcance. Os medidores que possuem esse método medem de 0 a 2,50 mg / L de fosfato (0 a 0,82 mg / L de fósforo).
Os métodos ácido ascórbico e aminoácido são essencialmente um processo em duas etapas. No primeiro estágio, o ortofosfato reage com o molibdato em uma solução ácida para formar um complexo amarelo de fosfomolibdato. O complexo fosfomolibdato é então reduzido usando um aminoácido ou ácido ascórbico, criando uma molécula que fará com que a amostra fique azul. A cor azul produzida é proporcional à concentração de fosfato na amostra.
Método Molibdovanadato
O Método Molibdovanadato é um processo de uma etapa. No método do molibdato, o molibdato reage sob condições ácidas com o ortofosfato para formar o ácido molibofosfórico. Na presença de vanádio, forma-se ácido ácido vanadomolibdofosfórico, de cor amarela. A intensidade desta cor amarela é proporcional à concentração de fosfato na amostra.
Diferentes formas de fosfatos / fósforo
Todos os métodos colorimétricos finalmente medem a quantidade de fosfato / fósforo na água em sua forma mais simples, o ortofosfato. Dependendo do medidor, a medição do ortofosfato é mostrada como fosfato e / ou fósforo. A preferência de ler de uma maneira ou de outra é baseada no padrão da indústria / mercado. Por exemplo, em aquários de água salgada, a preferência é ler como fosfato sobre fósforo. A diferença entre as duas medidas é apenas uma transformação matemática.
Como afirmado anteriormente, existem outros compostos de fósforo que podem ser medidos. Eles incluem fosfatos condensados e fósforo ligado organicamente e, para medir esses compostos, eles devem primeiro ser tratados para decompô-los da forma mais simples, o ortofosfato.
Fosfato condensado: teste de fósforo hidrolisável ácido
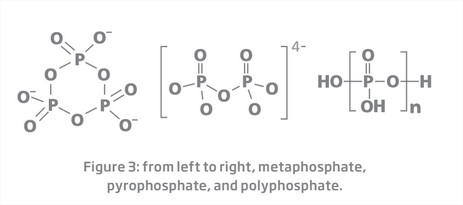
Concentração de fósforo condensado
Para determinar a concentração de fósforo condensado, é necessário digerir a amostra a 150 ° C com ácido sulfúrico por 30 minutos para converter qualquer forma condensada em ortofosfato. Devido ao uso de ácido como parte do processo de digestão, o parâmetro é relatado como fosfato hidrolisável por ácido. Para determinar a quantidade real de fosfato condensado em uma amostra, seria necessário subtrair a quantidade de ortofosfato de um teste de fósforo reativo do resultado do teste de fósforo hidrolisável por ácido.ácido hidrolisável – reagente = condensado
Fosfatos orgânicos – Teste de fósforo total
Os fosfatos orgânicos são grupos de ortofosfato que estão ligados a moléculas orgânicas. Um dos exemplos mais comuns é a molécula de adenosina trifosfato ou ATP. O ATP é comumente chamado de moeda energética da célula devido ao seu uso como transportador de energia em reações bioquímicas. Os fosfatos orgânicos surgem devido a processos biológicos, portanto, a medição da fração de fosfato orgânico fornece uma aproximação da atividade biológica.Para determinar a concentração total de fósforo, a amostra requer digestão a 150 ° C com ácido sulfúrico e persulfato de potássio por 30 minutos para converter todas as formas de fósforo (orgânico e condensado) em ortofosfato. Para medidores que medem o fósforo total, o método do ácido ascórbico é a base para medir a faixa baixa e o vandomolibovovanadato para a faixa alta.
A quantidade real de fosfato orgânico presente em uma amostra pode ser calculada subtraindo a quantidade de fósforo determinada pelo método de fósforo hidrolisável por ácido do resultado obtido por um teste de fósforo total. A diferença entre os dois resultados é a quantidade de fósforo que é organicamente ligada.
fósforo total – ácido hidrolisável = ligação orgânica
Fonte: Hanna
Você precisa de um medidor para realizar uma análise de fósforo? Clique Aqui